10a 2011 12: Unterschied zwischen den Versionen
Aus RMG-Wiki
K |
|||
| Zeile 117: | Zeile 117: | ||
'''2. Kurzarbeit: 15.06.2012''' <br> | '''2. Kurzarbeit: 15.06.2012''' <br> | ||
| − | '' | + | <br> |
| + | Hauptthema: '''Organische Chemie'''<br> | ||
| + | |||
| + | * 1. Benennung von organischen Verbindungen | ||
| + | * 2. Zusammenhang zwischen Struktur und Eigenschaften von organischen Verbindungen | ||
| + | |||
| + | Neben den Hefteinträgen und dem Versuchsprotokoll (s. unten: VP vom 17.04) eignen sich folgende Seiten im Buch zur Vorbereitung: | ||
| + | <br> | ||
| + | * Die Chemie der Kohlenstoffverbindungen (S. 90 - 91) | ||
| + | * Methan, der einfachste Kohlenwasserstoff (S. 94, nur der erste Abschnitt) | ||
| + | * Die homologe Reihe der Alkane (S. 96 - 97) | ||
| + | * Die Benennung der Alkane (S. 98 - 99) | ||
| + | * Die Familie der Alkane genauer betrachtet (S. 100 - 101) | ||
| + | * Kohlenwasserstoffe als Energieträger (S. 102 - 103) | ||
| + | * Die Benennung von sauerstoffhaltigen organischen Verbindungen (S. 126 - 127) | ||
| + | * Struktur und physikalische Eigenschaften (S. 140 - 141) | ||
| + | |||
<br> | <br> | ||
Version vom 29. Mai 2012, 08:25 Uhr
Mathematik 10
Biologie
Zum Unterricht
Referate
|
Externe links
Präsentationstechnik
Organisatorisches zu den Referaten
|
Chemie
Termine1. Kurzarbeit: 29.11.2011 - vorbei - 2. Kurzarbeit: 15.06.2012
Neben den Hefteinträgen und dem Versuchsprotokoll (s. unten: VP vom 17.04) eignen sich folgende Seiten im Buch zur Vorbereitung:
|
Externe links- keine links - |
Versuchsprotokolle zu den Übungen
|
Lösungen zu Aufgaben
|
|
|
Grundwissen Anorganische Chemie
Folgende Begriffe solltest Du erklären können:
Gemische
- homogene: Legierung, Lösung, Gasgemisch
- heterogene: Feststoffgemisch, Emulsion, Suspension, Nebel, Schaum, Rauch
- Trennverfahren: Filtration, Destillation, Chromatographie
Aggregatszustände
- Zustände: fest (s), flüssig (l), gasförmig (g)
- Zustandsänderungen: schmelzen - erstarren, verdampfen - kondensieren, sublimieren - resublimieren
Einteilung chemischer Reaktionen
- nach der Energieänderung: exotherm, endotherm, Aktivierungsenergie, freiwerdende Energie, aufzuwendende Energie, Katalysator
- nach der Umgruppierung der Teilchen: Synthese, Analyse, Umsetzung
Aufstellen chemischer Gleichungen
- Begriffe: Elementsymbol, chemische Formel, Reaktionspfeil, Index, Koeffizient
- molekular formulierte Elemente: Wasserstoff (H2), Stickstoff (N2), Sauerstoff (O2), Fluor (F2), Chlor (Cl2), Brom (Br2), Iod (I2)
Säuren und ihre Anionen
Säuren sind Stoffe, die Protonen (H+-Ionen) abgeben können.
Basen sind Stoffe, die Protonen aufnehmen können.
Ampholyte können sowohl Protonen aufnehmen, als auch abgeben
Beispiel: Hydrogenchlorid wird in Wasser geleitet
HCl + H2O 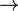 Cl- + H3O+
Cl- + H3O+
Beispiel: Ammoniak wird in Wasser geleitet
NH3 + H2O 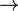 NH4+ + OH-
NH4+ + OH-
- Schwefelsäure (H2SO4): HSO4- Hydrogensulfat, SO42- Sulfat
- Kohlensäure (H2CO3): HCO3- Hydrogencarbonat, CO32- Carbonat
- Phosphorsäure (H3PO4): H2PO4- Dihydrogenphosphat, HPO42- Hydrogenphosphat, PO43- Phosphat
- Salpetersäure (HNO3): NO3- Nitrat </span>
Oxidation und Reduktion
- hier fehlt noch etwas!
Grundwissen Organische Chemie
- hier fehlt noch etwas!

