Physikalisches: Unterschied zwischen den Versionen
(typo) |
|||
| (92 dazwischenliegende Versionen von 8 Benutzern werden nicht angezeigt) | |||
| Zeile 1: | Zeile 1: | ||
| − | + | {{Projekt C14-Methode/Navigation}} | |
| + | __NOTOC__ | ||
| + | __NOEDITSECTION__ | ||
| + | {|width=100%| style="background-color: #436EEE; border: 0px solid #B4CDCD; padding:0.5em" | ||
| + | |<center> | ||
| + | {|width=80%| style="background-color:white; border: 0px solid #B0C4DE; padding: 0.5em; text-align:left" | ||
| + | |text-allign:"left"| | ||
| + | ==Grundlagen der C14-Methode== | ||
| + | |||
| + | Ziel der C14-Methode ist es, das Alter eines Gegenstandes zu bestimmen. Diese Methode eignet sich gegenüber den [[Projekt C14-Methode/Andere Datierungsmethoden | anderen Datierungsmöglichkeiten]] besonders wegen der leichteren Durchführung und eines besseren Messergebnisses. Doch zuerst muss man wissen was <sup>14</sup>C ist. | ||
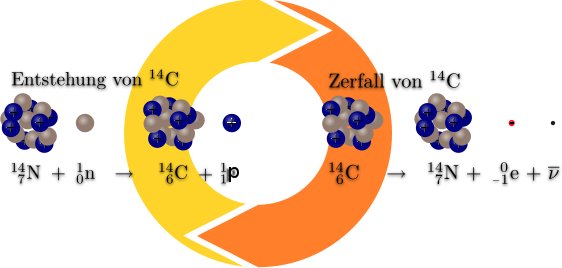
| − | + | <sup>14</sup>C ist ein [[Projekt C14-Methode/Physikon#Isotop | Isotop]] des Atoms <sup>12</sup>C. Es entsteht, wenn kosmische Strahlung (Neutronen) auf die Erdatmosphäre und dort Stickstoff-[[Projekt C14-Methode/Physikon#Isotop | Isotop]]e <sup>14</sup>N treffen. Es gibt eine Kernreaktion, in der <sup>14</sup>N zu <sup>14</sup>C unter Abgabe eines Protons zerfällt. | |
| − | |||
| − | |||
| − | + | :::''' <sup>14</sup>N + N ---------> <sup>14</sup>C+ P''' | |
| + | ::::::::::::N=Neutron | ||
| + | ::::::::::::P=Proton | ||
| − | |||
| − | |||
| − | |||
| − | ::: | + | ::[[Bild:C14-1.jpg.jpg| 600px]] |
| − | + | ||
| + | Es entsteht <sup>14</sup>C, das wieder zu Stickstoff zerfällt. | ||
| − | |||
| − | |||
| − | + | ||
| + | Das nun entstandene <sup>14</sup>C ist [[Projekt C14-Methode/Physikon#Radioaktive Strahlung | radioaktiv]] und zerfällt nach einer [[Projekt C14-Methode/Physikon#Halbwertszeit | Halbwertszeit]] von ca. 5730 Jahren unter Abgabe eines Elektrons | ||
| + | '''([[Projekt C14-Methode/Physikon#Radioaktive Strahlung |Beta-Zerfall]])''' zu <sup>14</sup>C.<br /> | ||
| + | |||
| + | |||
| + | ::::::::[[Bild: Betastrahlung.jpg|300px]] | ||
| + | |||
| + | |||
| + | |||
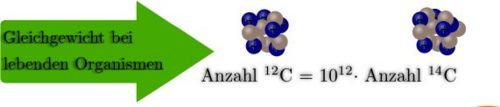
| + | Aufgrund von Luftströmungen verteilt sich das <sup>14</sup>C auf der ganzen Welt. Es reagiert mit dem Sauerstoff in der Atmosphäre zu <sup>14</sup>CO<sub>2</sub>. Durch die von Pflanzen betriebene [[Projekt C14-Methode/Physikon#Photosynthese | Photosynthese]] gelangt das <sup>14</sup>C nun in organisches Material. So nimmt auch der Mensch immer, wenn er etwas isst, einen winzig kleinen Teil <sup>14</sup>C auf, es stellt sich ein Gleichgewicht zwischen <sup>12</sup>C und <sup>14</sup>C ein. | ||
| + | |||
| + | [[Bild:C14-2.jpg.jpg| 500px]] | ||
| + | |||
| + | [[Bild:C14-3.jpg.jpg| 500px]] | ||
| + | |||
| + | |||
| + | |||
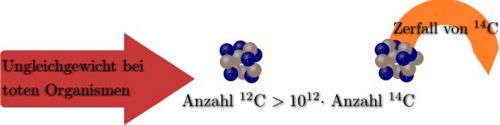
| + | Sobald das Lebewesen jedoch stirbt, verändert sich das Verhältnis zwischen <sup>14</sup>C und <sup>12</sup>C in seinem Körper. Da die [[Projekt C14-Methode/Physikon#Halbwertszeit | Halbwertszeit]] des Kohlenstoff[[Projekt C14-Methode/Physikon#Isotop |isotop]]s bekannt ist, kann man nun durch Messungen der [[Projekt C14-Methode/Physikon#Radioaktive Strahlung | radioaktiven Zerfälle]] auf das Alter der Probe schließen. Mit Hilfe der Massenspektrometrie und der Zählrohrmethode kann man das Verhältnis zwischen <sup>12</sup>C und <sup>14</sup>C herausfinden. Dies ist vor allem sinnvoll bei der Datierung von Werkstoffen, da sich das Problem ergibt, dass man mit möglichst wenig Material eine Datierung durchführen soll. | ||
| + | |} | ||
| + | </center> | ||
| + | |} | ||
| + | {|width=100%| style="background-color: #436EEE; border: 0px solid #B4CDCD; padding:0.5em" | ||
| + | |<center> | ||
| + | {|width=80%| style="background-color:white; border: 0px solid #B0C4DE; padding: 0.5em; text-align:left" | ||
| + | |text-allign:"left"| | ||
| + | ==Die Zählrohrmethode nach Libby== | ||
| + | |||
| + | Der direkte Nachweis des radioaktiven Zerfalls in einem [[Projekt C14-Methode/Physikon#Geiger-Müller Zählrohr | Geiger-Müller Zählrohr]] funktioniert so: | ||
| + | Zuerst muss die Probe verbrannt werden, es entsteht ein so genanntes Zählgas, das aus CO<sub>2</sub> besteht. Je nach dem, ob <sup>12</sup>C oder <sup>14</sup>C daran beteiligt war, ist dieses mehr oder weniger radioaktiv. Der [[Projekt C14-Methode/Physikon#Radioaktive Strahlung | radioaktive Zerfall]] ist ein statistischer Prozess, d.h. es zerfallen einmal mehr, einmal weniger Atome. Um die Zerfallsrate genau bestimmen zu können muss man daher möglichst viele Zerfälle messen. Um eine Genauigkeit von ±1% zu gewährleisten müssen 10 000 bis 40 000 Zerfälle erfasst werden. Ebenso muss das Zählrohr gut gegen die natürliche Strahlung abgeschirmt sein. | ||
| + | Da <sup>14</sup>C aber eine vergleichsweise lange [[Projekt C14-Methode/Physikon#Halbwertszeit | Halbwertszeit]] hat und die <sup>14</sup>C-Konzentration sehr gering ist erfordert die Zählrohrmethode große Probenmengen (einige Gramm) und lange Messzeiten, für eine dementsprechende Genauigkeit. Dadurch ergeben sich unter Umständen Messzeiten, die sich in der Größenordnung von Tagen und Wochen bewegen.<br /> | ||
| + | Vorteil: Relativ kleine, einfache und kostengünstige Apparatur. <br /> | ||
| + | Nachteile: Wegen der großen [[Projekt C14-Methode/Physikon#Halbwertszeit | Halbwertszeit]] von radioaktivem Kohlenstoff finden nur wenige Zerfälle statt, sodass lange Messzeiten erforderlich sind und große Probemengen benötigt werden (mindestens einige Gramm). | ||
| + | |} | ||
| + | </center> | ||
| + | |} | ||
| + | {|width=100%| style="background-color: #436EEE; border: 0px solid #B4CDCD; padding:0.5em" | ||
| + | |<center> | ||
| + | {|width=80%| style="background-color:white; border: 0px solid #B0C4DE; padding: 0.5em; text-align:left" | ||
| + | |text-allign:"left"| | ||
| + | ==Die Beschleuniger-Massenspektrometrie== | ||
| + | |||
| + | Die Beschleuniger-Massenspektrometrie ist ein technisches Verfahren mit dem man Massen-/[[Projekt C14-Methode/Physikon#Isotop | Isotop]]enverhältnisse, hier natürlich <sup>14</sup>C, eines Werkstoffes bestimmen kann. Der Vorteil dieser Methode ist, dass man auch mit einer sehr kleinen Menge, der zu messenden Substanz, ein genaues Ergebnis erzielt. | ||
| + | |||
| + | Bei der Spektrometrie wird die zu behandelnde Substanz zunächst in kleiner Menge und in Form von [[Projekt C14-Methode/Physikon#Ionisiertes Gas | ionisiertem Gas]] in einen Teilchenbeschleuniger gegeben. Im Beschleuniger wird die Substanz durch ein in [[Projekt C14-Methode/Physikon#Vakuum | Vakuum]] eingeschlossenes elektrisches Feld beschleunigt. So beschleunigt fliegen die Teilchen in einen sogenannten Massenspektrometer. Dieser besteht aus einem Magneten und einem Detektorsystem, wobei hier der Beschleuniger als Ionenquelle fungiert. Nachdem die Teilchen den Beschleuniger verlassen haben, treten diese in das Magnetfeld des Spektrometers. Dort werden die unterschiedlichen [[Projekt C14-Methode/Physikon#Isotop | Isotop]]e aufgrund ihrer jeweils spezifischen Flugbahn auch anders abgelenkt. Mit einem Detektor werden die Teilchenstrahlen gemessen, man kann den Stoff charakterisieren und auf den <sup>14</sup>C-Anteil „schließen“. Abschließend wird die Messung mit vorherigen Messergebnissen verglichen und man kann auf diese Art und Weise, wie bei allen anderen Methoden, das Alter des Ausgangsstoffes bestimmen. | ||
| + | |||
| + | Im folgenden Video wird die Massenspektrometrie noch einmal bildlich dargestellt: | ||
| + | |||
| + | :::::::::::{{#ev:youtube |onVfiL4yBZM|500}} | ||
| + | |||
| + | |} | ||
| + | </center> | ||
| + | |} | ||
| + | {|width=100%| style="background-color: #436EEE; border: 0px solid #B4CDCD; padding:0.5em" | ||
| + | |<center> | ||
| + | {|width=80%| style="background-color:white; border: 0px solid #B0C4DE; padding: 0.5em; text-align:left" | ||
| + | |text-allign:"left"| | ||
| + | == Probleme und Schwächen der Radiokohlenstoffdatierung == | ||
| + | |||
| + | Der <sup>14</sup>C-Gehalt der Atmosphäre im Verhältnis zum <sup>12</sup>C-Gehalt variiert, da sich die Sonnenaktivität im Laufe der Geschichte verändert hat. Aus diesem Grund ist es notwendig eine sogenannte [[Projekt C14-Methode/Physikon#Eichkurve|Eichkurve]] zu erstellen. Ein weiteres Problem ist die Tatsache, dass die Methode nicht auf sehr kleine Proben angewendet werden kann, da man einige Gramm <sup>14</sup>C benötigt um den Prozentsatz zu bestimmen. Außerdem zerfällt der Kohlenstoff je nach Ort und Zeitpunkt in verschiedener Geschwindigkeit. Allein dadurch ergeben sich Messfehler von bis zu 300 Jahren. Ein weiteres Problem ist die Radioaktive Verseuchung der Umgebung. Für Proben nach den ersten Atomwaffentests ist die C14-Methode nicht mehr anwendbar, da der Anteil an radioaktivem Material in der Atmosphäre vervielfacht wurde. Außerdem kann man die Methode nur für biologische Objekte wie zum Beispiel Pflanzen oder Tiere verwenden, da nur sie <sup>14</sup>C aufnehmen können. | ||
| + | |} | ||
| + | </center> | ||
| + | |} | ||
| + | {|width=100%| style="background-color: #436EEE; border: 0px solid #B4CDCD; padding:0.5em" | ||
| + | |<center> | ||
| + | {|width=80%| style="background-color:white; border: 0px solid #B0C4DE; padding: 0.5em; text-align:left" | ||
| + | |text-allign:"left"| | ||
| + | |||
| + | '''Weiterführende Links''': | ||
| + | |||
| + | 1. Wikipedia:[http://de.wikipedia.org/wiki/Radiokohlenstoffdatierung Radiokohlenstoffdatierung] | ||
| + | |||
| + | 2. Facharbeit zur <sup>14</sup>C-Methode:[http://www.c14methode.de.vu/ Facharbeit] | ||
| + | |||
| + | 3. [http://www.supplement.de/geographie/phygeo/c14.jpg Beispiel <sup>14</sup>C-Methode] | ||
| + | |||
| + | |} | ||
| + | </center> | ||
| + | |} | ||
| + | {|width=100%| style="background-color: #436EEE; border: 0px solid #B4CDCD; padding:0.5em" | ||
| + | |<center> | ||
| + | {|width=80%| style="background-color:white; border: 0px solid #B0C4DE; padding: 0.5em; text-align:left" | ||
| + | |text-allign:"left"| | ||
| + | [[Projekt C14-Methode/Physikon |'''Verzeichnis der physikalischen Fachbegriffe/ Physikon''']] | ||
| + | |} | ||
| + | </center> | ||
| + | |} | ||
Aktuelle Version vom 23. April 2012, 05:36 Uhr
| Hauptseite | |||||
|---|---|---|---|---|---|
| Physikalisches | Berufsfelder | Andere Methoden | Geschichte | Eigene Erfahrungen | Quiz |
|
|
|
|
|