Grundwissen Chemie: 10. Klasse NTG: Unterschied zwischen den Versionen
(kat) |
|||
| (12 dazwischenliegende Versionen von 2 Benutzern werden nicht angezeigt) | |||
| Zeile 1: | Zeile 1: | ||
| + | == Vorläufige Version! == | ||
| + | |||
Die Darstellung der Tabelle erfolgt nur optimal, wenn die Bildschirmauflösung in der Breite mehr als 1280 Pixel beträgt! | Die Darstellung der Tabelle erfolgt nur optimal, wenn die Bildschirmauflösung in der Breite mehr als 1280 Pixel beträgt! | ||
| Zeile 8: | Zeile 10: | ||
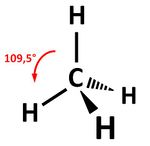
| Alkane <br> '''(---)'''|| [[Datei:RMGMethan1.jpg|150px]] || Methan || -an || radikalische <br> Substitution <br> Belichtung nötig! || Ethan + Brom <math>\longrightarrow </math> Bromethan + HBr <br> C<sub>2</sub>H<sub>6</sub> + Br<sub>2</sub> <math>\longrightarrow </math> C<sub>2</sub>H<sub>5</sub>Br + HBr | | Alkane <br> '''(---)'''|| [[Datei:RMGMethan1.jpg|150px]] || Methan || -an || radikalische <br> Substitution <br> Belichtung nötig! || Ethan + Brom <math>\longrightarrow </math> Bromethan + HBr <br> C<sub>2</sub>H<sub>6</sub> + Br<sub>2</sub> <math>\longrightarrow </math> C<sub>2</sub>H<sub>5</sub>Br + HBr | ||
|- | |- | ||
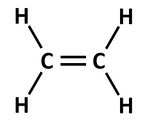
| − | | Alkene <br> '''(Doppelbindung)''' || [[Datei:RMGEthen1.jpg|150px]] || Ethen || -en || <span style="color:#0000CD"> '''elektrophile <br> Addition, | + | | Alkene <br> '''(Doppelbindung)''' || [[Datei:RMGEthen1.jpg|150px]] || Ethen || -en || <span style="color:#0000CD"> '''elektrophile <br> Addition,''' </span> || <span style="color:#0000CD">'''Ethen + Brom <math>\longrightarrow </math> 1,2-Dibromethan <br> C<sub>2</sub>H<sub>4</sub> + Br<sub>2</sub> <math>\longrightarrow </math> C<sub>2</sub>H<sub>4</sub>Br<sub>2</sub> <br> Hydrierung: <br> C<sub>2</sub>H<sub>4</sub> + H<sub>2</sub> <math>\longrightarrow </math> C<sub>2</sub>H<sub>6</sub>''' </span> |
| + | |- | ||
| + | | || || || || <span style="color:#CD0000"> '''Polymerisation''' </span> || <span style="color:#CD0000">'''C<sub>2</sub>H<sub>4</sub>''' <math>\longrightarrow </math> '''(-CH<sub>2</sub>-CH<sub>2</sub>-)<sub>n</sub></span>''' | ||
|- | |- | ||
| Alkine <br> '''(Dreifachbindung)'''|| [[Datei:RMGEthin1.jpg|150px]] || Ethin || -in || elektrophile <br> Addition, <br> Polymerisation || ''s. Alkene'' | | Alkine <br> '''(Dreifachbindung)'''|| [[Datei:RMGEthin1.jpg|150px]] || Ethin || -in || elektrophile <br> Addition, <br> Polymerisation || ''s. Alkene'' | ||
| Zeile 16: | Zeile 20: | ||
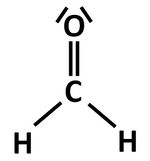
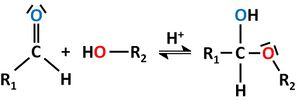
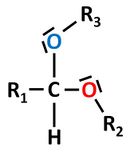
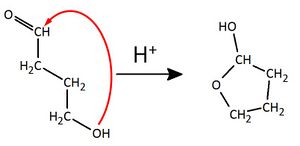
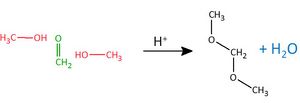
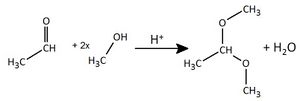
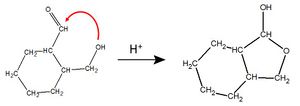
| Aldehyde <br> '''(endständige <br> Carbonylgruppe)'''|| [[Datei:RMGMethanal1.jpg|150px]] || Methanal <br> (Formaldehyd) || -al || nukleophile <br> Addition || Bildung von '''Halbacetalen''': <br> [[Datei:RMGHalbacetalbildung1.jpg|300px]] <br> Mit einem weiteren Alkohol <br> bildet sich unter Wasserabspaltung <br> ein '''Vollacetal''' <br> [[Datei:RMGVollacetal1.jpg|130px]] | | Aldehyde <br> '''(endständige <br> Carbonylgruppe)'''|| [[Datei:RMGMethanal1.jpg|150px]] || Methanal <br> (Formaldehyd) || -al || nukleophile <br> Addition || Bildung von '''Halbacetalen''': <br> [[Datei:RMGHalbacetalbildung1.jpg|300px]] <br> Mit einem weiteren Alkohol <br> bildet sich unter Wasserabspaltung <br> ein '''Vollacetal''' <br> [[Datei:RMGVollacetal1.jpg|130px]] | ||
|- | |- | ||
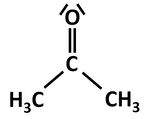
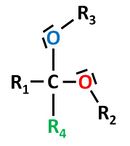
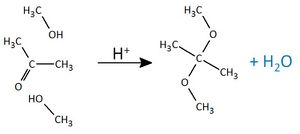
| − | | Ketone <br> '''(Carbonylgruppe)'''|| [[Datei:RMGPropanon.jpg|150px]] || Propanon <br> (Aceton) || - | + | | Ketone <br> '''(Carbonylgruppe)'''|| [[Datei:RMGPropanon.jpg|150px]] || Propanon <br> (Aceton) || -on || nukleophile <br> Addition || ''- wie Halbacetalbildung, nur ist die <br> Carbonylgruppe nicht endständig -'' <br> Es entstehen Halbketale und '''Vollketale''': <br> [[Datei:RMGVollketal.jpg|130px]] |
| + | |- | ||
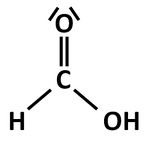
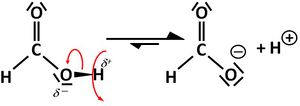
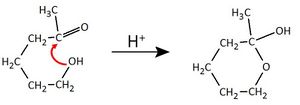
| + | | Carbonsäuren <br> '''(Carboxygruppe)'''|| [[Datei:RMGAmeisensäure.jpg|150px]] || Methansäure <br> (Ameisensäure) || -säure || Abspaltung von <br> Protonen (H<sup>+</sup>) || Carbonsäuren sind in der Regel '''schwache Säuren'''. <br> Die sich bildenden '''Carboxylat-Ionen''' <br> können wieder Protonen aufnehmen <br> und zurück zur Säure reagieren. <br> Es liegt ein '''dynamisches, chemisches Gleichgewicht''' vor: <br> [[Datei:RMGSäure_ProtonAbgabe1.jpg|300px]] | ||
|- | |- | ||
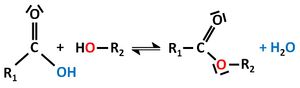
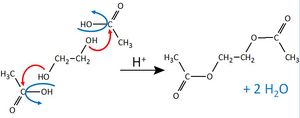
| − | | | + | | || || || || Esterkondensation || Essigsäure und Ethanol <math>\longrightarrow </math> Essigsäureethylester + Wasser <br> <br> ''Allgemein gilt:'' <br> [[Datei:RMGVeresterung1.jpg|300px]] |
|} | |} | ||
</center> | </center> | ||
| Zeile 55: | Zeile 61: | ||
{{versteckt| | {{versteckt| | ||
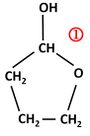
| − | Es handelt sich hierbei um eine Verbindung, die durch intramolekulare Halbacetalbildung aus 4-Hydroxbutanal hervorgegangen ist <br> [[Datei:RMGHalbacetal_Bsp1_ML.jpg| | + | Es handelt sich hierbei um eine Verbindung, die durch intramolekulare Halbacetalbildung aus 4-Hydroxbutanal hervorgegangen ist <br> [[Datei:RMGHalbacetal_Bsp1_ML.jpg|300px]] |
}} | }} | ||
</div><br> | </div><br> | ||
| Zeile 65: | Zeile 71: | ||
{{versteckt| | {{versteckt| | ||
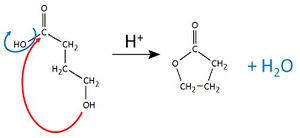
| − | Es handelt sich hierbei um einen intramolekularen Ester (sog. Lacton), der durch die Reaktion der Hydroxgruppe von 4-Hydroxybutansäure mit der Carboxgruppe entsteht. Dabei wird wie bei anderen säurekatalysierten Esterbildungen auch Wasser abgespalten <br> [[Datei:RMGintrMolEster_Bsp1_ML.jpg| | + | Es handelt sich hierbei um einen intramolekularen Ester (sog. Lacton), der durch die Reaktion der Hydroxgruppe von 4-Hydroxybutansäure mit der Carboxgruppe entsteht. Dabei wird wie bei anderen säurekatalysierten Esterbildungen auch Wasser abgespalten <br> [[Datei:RMGintrMolEster_Bsp1_ML.jpg|300px]] |
}} | }} | ||
</div><br> | </div><br> | ||
| Zeile 75: | Zeile 81: | ||
{{versteckt| | {{versteckt| | ||
| − | Auch hier liegt eine intramolekulare Reaktion von 5-Hydroxypentan-2-on vor. <br> [[Datei:RMGHalbetal_Bsp1_ML.jpg| | + | Auch hier liegt eine intramolekulare Reaktion von 5-Hydroxypentan-2-on vor. <br> [[Datei:RMGHalbetal_Bsp1_ML.jpg|300px]] |
}} | }} | ||
</div><br> | </div><br> | ||
| Zeile 85: | Zeile 91: | ||
{{versteckt| | {{versteckt| | ||
| − | Ein Vollacetal aus Methanal (Formaldehyd) und 2 Methanol-Molekülen <br> [[Datei:RMGVollacetal_Bsp2_ML.jpg| | + | Ein Vollacetal aus Methanal (Formaldehyd) und 2 Methanol-Molekülen <br> [[Datei:RMGVollacetal_Bsp2_ML.jpg|300px]] |
}} | }} | ||
</div><br> | </div><br> | ||
| Zeile 95: | Zeile 101: | ||
{{versteckt| | {{versteckt| | ||
| − | Ein Vollketal aus Propanon (Aceton) und 2 Methanol-Moleküle. <br> [[Datei:RMGVollketal_Bsp2_ML.jpg| | + | Ein Vollketal aus Propanon (Aceton) und 2 Methanol-Moleküle. <br> [[Datei:RMGVollketal_Bsp2_ML.jpg|300px]] |
}} | }} | ||
</div><br> | </div><br> | ||
| Zeile 110: | Zeile 116: | ||
{{versteckt| | {{versteckt| | ||
| − | Damit sich dieses Molekül bildet, müssen Pentan-2-on, Ethanol und Methanol miteinander reagieren! <br> [[Datei:RMGVollketal_Bsp1_ML.jpg| | + | Damit sich dieses Molekül bildet, müssen Pentan-2-on, Ethanol und Methanol miteinander reagieren! <br> [[Datei:RMGVollketal_Bsp1_ML.jpg|300px]] |
}} | }} | ||
</div><br> | </div><br> | ||
| Zeile 120: | Zeile 126: | ||
{{versteckt| | {{versteckt| | ||
| − | Bei diesem Vollacetal reagierte Ethanal zweimal mit Methanol. Bei der Reaktion von der Zwischenstufe "Halbacetal" zum Vollacetal wird Wasser abgespalten. <br> [[Datei:RMGVollacetal_Bsp1_ML.jpg| | + | Bei diesem Vollacetal reagierte Ethanal zweimal mit Methanol. Bei der Reaktion von der Zwischenstufe "Halbacetal" zum Vollacetal wird Wasser abgespalten. <br> [[Datei:RMGVollacetal_Bsp1_ML.jpg|300px]] |
}} | }} | ||
</div><br> | </div><br> | ||
| Zeile 130: | Zeile 136: | ||
{{versteckt| | {{versteckt| | ||
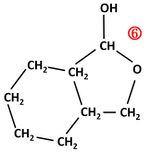
| − | Im Prinzip wie bei '''Verbindung 1''', die Ausgangsverbindung enthält nur einen zusätzlichen 6-Ring. Den Namen dieser Ausgangsverbindung muss man in der 10. Klasse noch nicht ableiten können: 2-(Hydroxymethyl)cyclohexancarbaldehyd. <br> [[Datei:RMGHalbacetal_Bsp2_ML.jpg| | + | Im Prinzip wie bei '''Verbindung 1''', die Ausgangsverbindung enthält nur einen zusätzlichen 6-Ring. Den Namen dieser Ausgangsverbindung muss man in der 10. Klasse noch nicht ableiten können: 2-(Hydroxymethyl)cyclohexancarbaldehyd. <br> [[Datei:RMGHalbacetal_Bsp2_ML.jpg|300px]] |
}} | }} | ||
</div><br> | </div><br> | ||
| Zeile 140: | Zeile 146: | ||
{{versteckt| | {{versteckt| | ||
| − | Diese Verbindung könnte entstehen, wenn 2 Essigsäuremoleküle mit Ethandiol reagieren.<br> [[Datei:RMGintrMolEster_Bsp2_ML.jpg| | + | Diese Verbindung könnte entstehen, wenn 2 Essigsäuremoleküle mit Ethandiol reagieren.<br> [[Datei:RMGintrMolEster_Bsp2_ML.jpg|300px]] |
}} | }} | ||
</div><br> | </div><br> | ||
| Zeile 150: | Zeile 156: | ||
{{versteckt| | {{versteckt| | ||
| − | Es handelt sich hierbei um eine Verbindung, die durch intramolekulare Halbacetalbildung aus 4-Hydroxbutanal hervorgegangen ist <br> [[Datei: | + | Es handelt sich hierbei um eine Verbindung, die durch intramolekulare Halbacetalbildung aus 4-Hydroxbutanal hervorgegangen ist <br> [[Datei:RMGHalbketal_Bsp2_MLV2.jpg|300px]] |
}} | }} | ||
</div><br> | </div><br> | ||
|} | |} | ||
| + | |||
| + | == Quiz zur Überprüfung 2 == | ||
| + | |||
| + | Die abgebildete Säure soll mit Natriumhydroxid reagieren. Gesucht ist der '''IUPAC-Name des entstehenden Salzes''' (Der Buchstaben-/Zeichensalat nach dem Eingabefeld kann zur Orientierung genutzt werden). Die vorgeschriebene Zeichensetzung ist zu berücksichtigen! Sobald in alle Eingabefelder ein Name eingegeben ist, erscheint ein Button, mit dem die Richtigkeit geprüft werden kann. | ||
| + | |||
| + | <div class="schuettel-quiz"> | ||
| + | |||
| + | [[Datei:RMGSäSalzBenenn1.jpg|300px]] heißt: '''Natrium-4-hydroxypentanoat''' <br> | ||
| + | [[Datei:RMGSäSalzBenenn2.jpg|300px]] heißt: '''Natrium-3,4-dihydroxypentanoat''' <br> | ||
| + | [[Datei:RMGSäSalzBenenn3.jpg|300px]] heißt: '''Natrium-3,3-dimethylbutanoat''' <br> | ||
| + | [[Datei:RMGSäSalzBenenn4.jpg|300px]] heißt: '''Natrium-3-hydroxy-3-methylbutanoat''' <br> | ||
| + | |||
| + | </div> | ||
| + | |||
| + | |||
| + | [[Kategorie:10. Klasse]] | ||
| + | [[Kategorie:Grundwissen Chemie]] | ||
| + | [[Kategorie:RMG2Edutags]] | ||
| + | <metakeywords>RMG2Edutags,RMG-Wiki,ZUM.de,OER,Grundwissen Chemie: 10. Klasse NTG,Grundwissen,Chemie,10. Klasse</metakeywords> | ||
Aktuelle Version vom 15. Oktober 2014, 22:31 Uhr
Vorläufige Version!
Die Darstellung der Tabelle erfolgt nur optimal, wenn die Bildschirmauflösung in der Breite mehr als 1280 Pixel beträgt!
Quiz zur Überprüfung
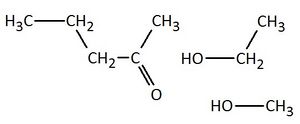
Ordne die unten abgebildeten Verbindungen durch Ziehen mit der Maus der richtigen Stoffgruppe zu!
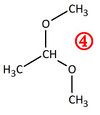
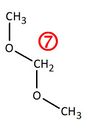
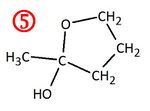
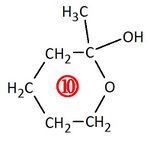
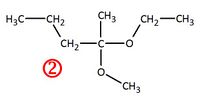
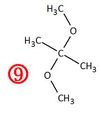
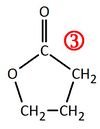
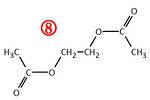
Versuche die Edukte zu zeichnen, bzw. zu benennen, die zu der nummerierten Verbindung geführt haben!
Durch Klicken auf Anzeigen wird die Lösung angezeigt!
Verbindung 1
Verbindung 3
|
Verbindung 2
Verbindung 4
Verbindung 6
Verbindung 10
|
Quiz zur Überprüfung 2
Die abgebildete Säure soll mit Natriumhydroxid reagieren. Gesucht ist der IUPAC-Name des entstehenden Salzes (Der Buchstaben-/Zeichensalat nach dem Eingabefeld kann zur Orientierung genutzt werden). Die vorgeschriebene Zeichensetzung ist zu berücksichtigen! Sobald in alle Eingabefelder ein Name eingegeben ist, erscheint ein Button, mit dem die Richtigkeit geprüft werden kann.
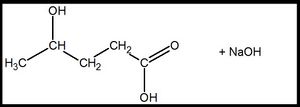 heißt: Natrium-4-hydroxypentanoat
heißt: Natrium-4-hydroxypentanoat
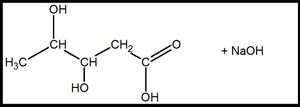 heißt: Natrium-3,4-dihydroxypentanoat
heißt: Natrium-3,4-dihydroxypentanoat
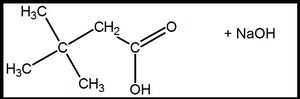 heißt: Natrium-3,3-dimethylbutanoat
heißt: Natrium-3,3-dimethylbutanoat
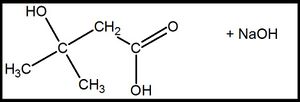 heißt: Natrium-3-hydroxy-3-methylbutanoat
heißt: Natrium-3-hydroxy-3-methylbutanoat
 Bromethan + HBr
Bromethan + HBr