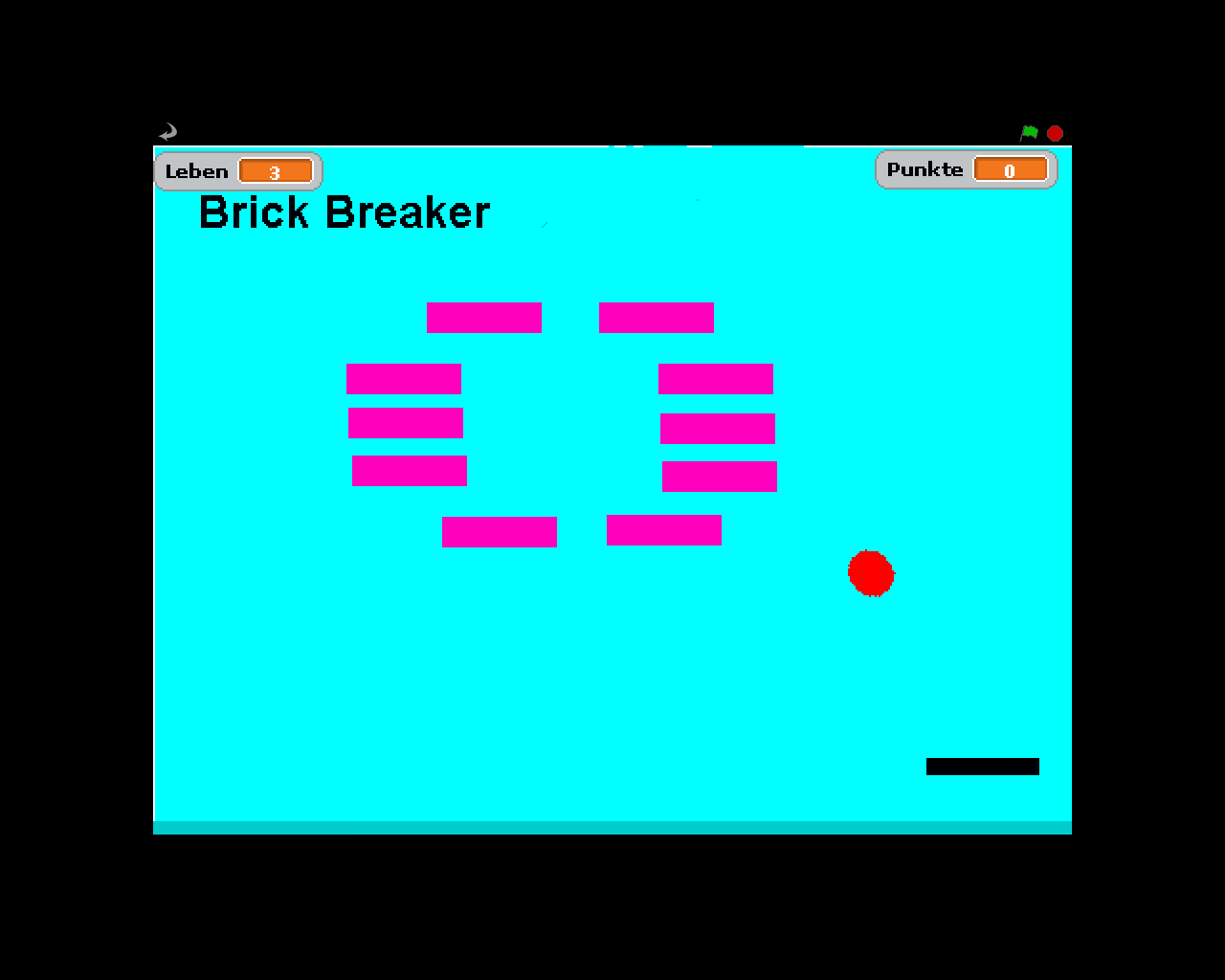
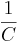Aufbau der Materie und Wärmelehre: Unterschied zwischen den Versionen
K (Layout) |
(layout) |
||
| Zeile 1: | Zeile 1: | ||
| − | == Aufbau der Materie und | + | == Aufbau der Materie und innere Energie== |
| + | |||
{|width=100%| style="background-color:lightblue; border: 1px solid #dfdfdf; padding:0.5em" | {|width=100%| style="background-color:lightblue; border: 1px solid #dfdfdf; padding:0.5em" | ||
| valign="top" | | | valign="top" | | ||
| − | + | fehlt noch | |
| − | + | ||
|} | |} | ||
| + | == Änderung der inneren Energie == | ||
{|width=100%| style="background-color:lightblue; border: 1px solid #dfdfdf; padding:0.5em" | {|width=100%| style="background-color:lightblue; border: 1px solid #dfdfdf; padding:0.5em" | ||
| valign="top" | | | valign="top" | | ||
| − | + | ||
'''Wärme:''' | '''Wärme:''' | ||
Symbol: Q | Symbol: Q | ||
| Zeile 21: | Zeile 22: | ||
In einem abgeschlossenem System ist die Änderung der inneren Energie verbunden mit der Zufuhr oder Abgabe von Wärme und dem Verrichten mechanischer Arbeit. | In einem abgeschlossenem System ist die Änderung der inneren Energie verbunden mit der Zufuhr oder Abgabe von Wärme und dem Verrichten mechanischer Arbeit. | ||
| − | |||
| − | |||
'''ΔEi=W+Q''' | '''ΔEi=W+Q''' | ||
| Zeile 31: | Zeile 30: | ||
| + | == Energieentwertung == | ||
{|width=100%| style="background-color:lightblue; border: 1px solid #dfdfdf; padding:0.5em" | {|width=100%| style="background-color:lightblue; border: 1px solid #dfdfdf; padding:0.5em" | ||
| valign="top" | | | valign="top" | | ||
| + | === Reversible und irreversible Vorgänge === | ||
| + | Ein Vorgang in Natur und/oder Technik kann reversibel oder irreversibel verlaufen. Das bedeutet: | ||
| − | |||
| − | + | '''reversible Vorgänge'''[[Bild:Fadenpendel.JPG|200px|right]] | |
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | [[Bild: | + | |
| − | ====Wirkungsgrad bei | + | |
| + | ein reversibler Vorgang ist umkehrbar, d. h. der Ausgangszustand wird von allein wieder erreicht | ||
| + | |||
| + | |||
| + | |||
| + | Beispiel: Bewegung der Erde um die Sonne, Fadenpendel (bei kurzer Dauer) | ||
| + | |||
| + | |||
| + | |||
| + | |||
| + | |||
| + | |||
| + | |||
| + | |||
| + | |||
| + | |||
| + | |||
| + | |||
| + | |||
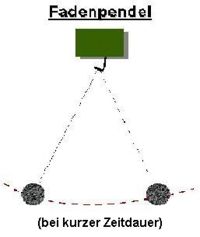
| + | '''irreversible Vorgänge'''[[Bild:Energiebilanz.jpg|400px|right]] | ||
| + | |||
| + | |||
| + | ein irreversibler Vorgang ist '''NICHT''' umkehrbar, d.h. der Ausgangszustand kann von alleine '''NICHT''' wieder erreicht werden. | ||
| + | |||
| + | |||
| + | |||
| + | Beispiel: Verbrennen eines Stoffes | ||
| + | |||
| + | |||
| + | |} | ||
| + | |||
| + | |||
| + | {|width=100%| style="background-color:lightblue; border: 1px solid #dfdfdf; padding:0.5em" | ||
| + | |valign="top" | | ||
| + | ===Wirkungsgrad bei irreversiblen Vorgängen=== | ||
Bei allen irreversiblen Vorgängen wird Energie in Form von Wärme entwertet. Der Wirkungsgrad bei allen Vorgängen, bei denen auch die Innere Energie eine Rolle spielt, ist immer kleiner als 100%, da Innere Energie nie vollständig in andere Energieformen umgewandelt werden kann. | Bei allen irreversiblen Vorgängen wird Energie in Form von Wärme entwertet. Der Wirkungsgrad bei allen Vorgängen, bei denen auch die Innere Energie eine Rolle spielt, ist immer kleiner als 100%, da Innere Energie nie vollständig in andere Energieformen umgewandelt werden kann. | ||
| Zeile 62: | Zeile 89: | ||
| + | == Volumenänderung bei Temperaturänderung == | ||
{|width=100%| style="background-color:lightblue; border: 1px solid #dfdfdf; padding:0.5em" | {|width=100%| style="background-color:lightblue; border: 1px solid #dfdfdf; padding:0.5em" | ||
| valign="top" | | | valign="top" | | ||
| − | + | ===Volumenänderung von Flüssigkeiten=== | |
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
(Daniel H.<-Hat alles alleine gemacht,Patrik H.,Sebastian B.,Christoph Z.) | (Daniel H.<-Hat alles alleine gemacht,Patrik H.,Sebastian B.,Christoph Z.) | ||
| Zeile 79: | Zeile 102: | ||
| − | + | '''Volumenausdehnungskoeffizienten Beispiele (γ in l/°C bei 20 °C ):''' | |
Benzin: 0,0010 | Benzin: 0,0010 | ||
| Zeile 93: | Zeile 116: | ||
Alkohol: 0,0011 | Alkohol: 0,0011 | ||
| − | Beispiel: | + | |
| + | |||
| + | Beispiel: | ||
Berechne die Volumenänderung von 76 LiterBenzin wenn sie sich von 10°C auf 20°C erwärmen | Berechne die Volumenänderung von 76 LiterBenzin wenn sie sich von 10°C auf 20°C erwärmen | ||
Gegeben: | Gegeben: | ||
| − | + | V<sub>0</sub>=76 l; γ = 0,0010 l/°C; Δδ = 10°C | |
Gesucht: | Gesucht: | ||
| − | + | Δ V | |
Lösung: | Lösung: | ||
| − | + | ΔV = V<sub>0</sub>*y*Δδ | |
= 76l * 0,0010 l/°C * 10°C | = 76l * 0,0010 l/°C * 10°C | ||
| − | = 0, | + | = 0,76 l |
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
| − | + | ||
|} | |} | ||
| − | |||
| − | |||
| − | |||
| + | {|width=100%| style="background-color:lightblue; border: 1px solid #dfdfdf; padding:0.5em" | ||
| + | | | ||
| + | ===Längenänderung von Festkörpern=== | ||
Alle Festkörper dehnen sich bei Erwärmung aus, jedoch nicht alle gleichmäßig (linear). Dafür ist der jeweilige Längenausdehnungskoeffizient verantwortlich. Dieser ist bei jedem Stoff anders. Es kann berechnet werden, um wie viel cm sich ein Stoff ausdehnt und zwar mit dieser Formel: | Alle Festkörper dehnen sich bei Erwärmung aus, jedoch nicht alle gleichmäßig (linear). Dafür ist der jeweilige Längenausdehnungskoeffizient verantwortlich. Dieser ist bei jedem Stoff anders. Es kann berechnet werden, um wie viel cm sich ein Stoff ausdehnt und zwar mit dieser Formel: | ||
| Zeile 219: | Zeile 215: | ||
|0,000 002 | |0,000 002 | ||
|} | |} | ||
| + | |||
|} | |} | ||
| − | {|width=100%| style="background-color: | + | |
| + | {|width=100%| style="background-color:lightblue; border: 1px solid #dfdfdf; padding:0.5em" | ||
| valign="top" | | | valign="top" | | ||
| + | ===Anomalie des Wassers=== | ||
| − | ==== Volumenänderung von Gasen | + | '''Dichte:''' |
| + | |||
| + | Wasser hat unter Normaldruck seine größte Dichte von bei ca. 4°C und zeigt damit eine Dichteanomalie. | ||
| + | Diese besteht darin, dass sich Wasser unterhalb von ca. 4°C bei weiterer Temperaturverringerung, auch beim Wechsel zum festen Aggregatzustand, wieder ausdehnt, was man nur von wenigen Stoffen kennt. | ||
| + | Dies führt dazu, dass Eisberge schwimmen. | ||
| + | Im flüssigen Zustand herrscht eine Mischung von Ordnung und Chaos, wobei die Moleküle aufgrund ihrer höheren Geschwindigkeit ein größeres Volumen ausfüllen. | ||
| + | Es erhöht sich also das Volumen und die Dichte wird damit geringer. | ||
| + | Im gasförmigen Zustand ist die maximale Unordnung erreicht und die Atome verteilen sich dementsprechend gleichmäßig über den maximal zur Verfügung stehenden Raum. | ||
| + | Festes Wasser hat eine geringere Dichte als flüssiges Wasser, es schwimmt (=anomales Verhalten). | ||
| + | |||
| + | '''Es gilt:''' | ||
| + | |||
| + | -je größer die Temperatur des Wassers, desto kleiner die Dichte | ||
| + | |||
| + | -je kleiner die Temperatur des Wassers, desto größer die Dichte | ||
| + | |||
| + | '''Außer''':[[Bild:AnomalieWasser.jpg|right]] | ||
| + | |||
| + | |||
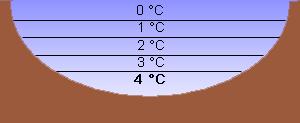
| + | Ab 4°C wird das Volumen nicht kleiner sondern bis 0°C wieder größer. | ||
| + | Wasser hat bei 4°C die größte Dichte. | ||
| + | |||
| + | |||
| + | |} | ||
| + | |||
| + | |||
| + | {|width=100%| style="background-color:lightblue; border: 1px solid #dfdfdf; padding:0.5em" | ||
| + | | | ||
| + | === Volumenänderung von Gasen === | ||
Alle Gase dehnen sich unter Wärmezufuhr ungefähr gleich aus, vorrausgesetzt sie besitzen die gleiche Ausgangstemperatur und stehen unter gleichem Druck. Folglich gilt: | Alle Gase dehnen sich unter Wärmezufuhr ungefähr gleich aus, vorrausgesetzt sie besitzen die gleiche Ausgangstemperatur und stehen unter gleichem Druck. Folglich gilt: | ||
| Zeile 231: | Zeile 258: | ||
Allerdings gibt es keine Formel mit der man die Ausdehnung genau berechnen kann. | Allerdings gibt es keine Formel mit der man die Ausdehnung genau berechnen kann. | ||
| − | |||
|} | |} | ||
Version vom 11. Juli 2008, 20:58 Uhr
Inhaltsverzeichnis |
Aufbau der Materie und innere Energie
|
fehlt noch |
Änderung der inneren Energie
|
Wärme: Symbol: Q Einheit: 1J=1(kg*m²)/s² Grundgleichung der Wärmelehre bei Erwärmen oder Abkühlen von Körpern ohne Aggregatszustandsänderung:
Q=c*m*Δ 1.Hauptsatz der Wärmlehre: In einem abgeschlossenem System ist die Änderung der inneren Energie verbunden mit der Zufuhr oder Abgabe von Wärme und dem Verrichten mechanischer Arbeit. ΔEi=W+Q ΔEi:Änderung der inneren Energie
W:Verrichten mechanischer Arbeit
Q:Abgabe/Zufuhr von Wärme
|
Energieentwertung
Reversible und irreversible VorgängeEin Vorgang in Natur und/oder Technik kann reversibel oder irreversibel verlaufen. Das bedeutet:
Beispiel: Bewegung der Erde um die Sonne, Fadenpendel (bei kurzer Dauer)
Beispiel: Verbrennen eines Stoffes
|
Wirkungsgrad bei irreversiblen VorgängenBei allen irreversiblen Vorgängen wird Energie in Form von Wärme entwertet. Der Wirkungsgrad bei allen Vorgängen, bei denen auch die Innere Energie eine Rolle spielt, ist immer kleiner als 100%, da Innere Energie nie vollständig in andere Energieformen umgewandelt werden kann. Folglich tritt immer eine Energieentwertung auf. Beispiel: Ein laufender Motor erhitzt sich. Die Wärmeenergie wird durch die Verbrennung des Treibstoffs erzeugt, allerdings kann sie nicht zum Antreiben des Fahrzeugs verwendet werden.
Hier findest du Aufgaben dazu: |
Volumenänderung bei Temperaturänderung
Volumenänderung von Flüssigkeiten(Daniel H.<-Hat alles alleine gemacht,Patrik H.,Sebastian B.,Christoph Z.) Flüssigkeiten (ausser Wasser) dehnen sich bei konstanter Temperaturerhöhung linear aus. Volumenausdehnung = Ausgangsvolumen * Volumenausdehnungskoeffizient * Temperaturdifferenz
Benzin: 0,0010 Wasser: 0,00021 Quecksilber: 0,00018 Petroleum: 0,0009 Heizöl: 0,0009 Alkohol: 0,0011
Beispiel: Berechne die Volumenänderung von 76 LiterBenzin wenn sie sich von 10°C auf 20°C erwärmen Gegeben: V0=76 l; γ = 0,0010 l/°C; Δδ = 10°C Gesucht: Δ V Lösung: ΔV = V0*y*Δδ = 76l * 0,0010 l/°C * 10°C = 0,76 l |
Längenänderung von FestkörpernAlle Festkörper dehnen sich bei Erwärmung aus, jedoch nicht alle gleichmäßig (linear). Dafür ist der jeweilige Längenausdehnungskoeffizient verantwortlich. Dieser ist bei jedem Stoff anders. Es kann berechnet werden, um wie viel cm sich ein Stoff ausdehnt und zwar mit dieser Formel: Δl = α * lo * Δδ oder: Volumenänderung = Volumenänderugskoeffizient * Ausgangslänge * Temperaturänderung
|
Anomalie des WassersDichte: Wasser hat unter Normaldruck seine größte Dichte von bei ca. 4°C und zeigt damit eine Dichteanomalie. Diese besteht darin, dass sich Wasser unterhalb von ca. 4°C bei weiterer Temperaturverringerung, auch beim Wechsel zum festen Aggregatzustand, wieder ausdehnt, was man nur von wenigen Stoffen kennt. Dies führt dazu, dass Eisberge schwimmen. Im flüssigen Zustand herrscht eine Mischung von Ordnung und Chaos, wobei die Moleküle aufgrund ihrer höheren Geschwindigkeit ein größeres Volumen ausfüllen. Es erhöht sich also das Volumen und die Dichte wird damit geringer. Im gasförmigen Zustand ist die maximale Unordnung erreicht und die Atome verteilen sich dementsprechend gleichmäßig über den maximal zur Verfügung stehenden Raum. Festes Wasser hat eine geringere Dichte als flüssiges Wasser, es schwimmt (=anomales Verhalten). Es gilt: -je größer die Temperatur des Wassers, desto kleiner die Dichte -je kleiner die Temperatur des Wassers, desto größer die Dichte Außer:
|
Volumenänderung von GasenAlle Gase dehnen sich unter Wärmezufuhr ungefähr gleich aus, vorrausgesetzt sie besitzen die gleiche Ausgangstemperatur und stehen unter gleichem Druck. Folglich gilt: Je wärmer ein Gas ist, desto größer sein Volumen. Allerdings gibt es keine Formel mit der man die Ausdehnung genau berechnen kann. |